| Thema: Salze und Salzbildung | Tags: Calciumchlorid, Natriumcarbonat, Konzentrationsunterschiede, Dichte | Klassenstufen: 9-10 | Versuchsart: SV |
Materialien
Petrischale, Spatel
Chemikalien
Wasser, Calciumchlorid-Dihydrat, Natriumcarbonat-Decahydrat
Durchführung
Die Petrischale wird bis zur Hälfte mit Wasser gefüllt. An einer Stelle wird nahe des Randes eines der beiden Salze vorsichtig in das Wasser gegeben. Auf gegenüberliegender Seite wird, ähnlich positioniert, ohne das Wasser in Bewegung zu bringen, das zweite Salz eingebracht.
Beobachtung
Die Salze lösen sich. Etwa mittig zwischen den Stellen, an denen das Salz positioniert wurde, bildet sich ein weißer Feststoff.
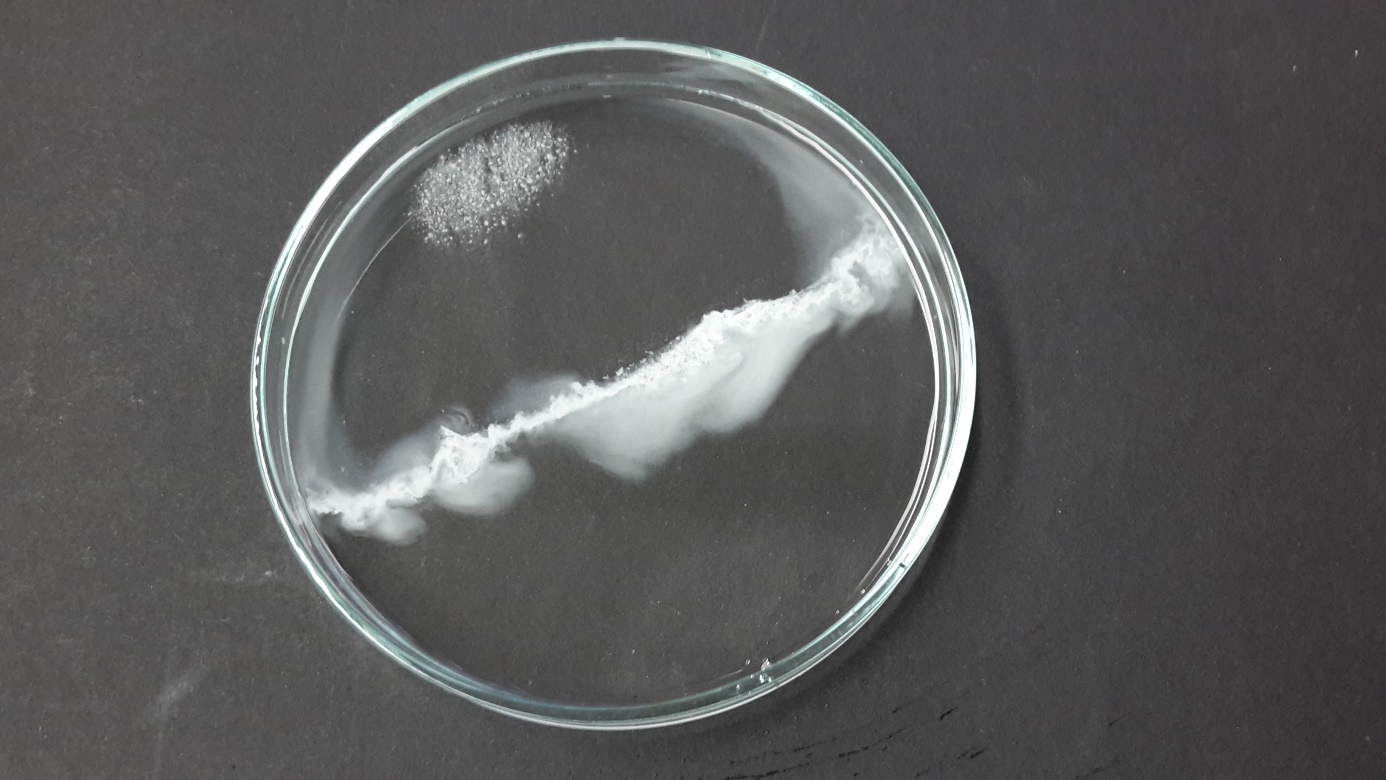
Deutung
Nachdem sich die Salze gelöst haben, sinken die Salzlösungen aufgrund ihrer hohen Dichte auf den Grund der Schale und breiten sich aus. Aufgrund der unterschiedlichen Dichte vermischen sich die Salzlösungen nicht mit dem Wasser. Bei Zusammentreffen der Lösungen reagieren diese miteinander zu Calciumcarbonat:
CaCl2 (aq) + Na2CO3 (aq) → CaCO3 (s) + 2 NaCl (aq).
Entsorgung
Die Entsorgung kann im Abfluss erfolgen.
Literatur
H. Schmidkunz, Chemische Freihandversuche, Kleine Versuche mit großer Wirkung, Aulis Verlag, 2011, S. 273.
Feedback
Haben Sie Anmerkungen, Feedback oder Kritik zu diesem Experiment? Kontaktieren Sie uns unter Bezugnahme auf diese Seite!
Copyright und Lizenzen: Alle Rechte an den Inhalten dieser eLearning-Materialien liegen beim Autor oder den jeweiligen Urheberrechtsinhabern. Sämtliche Bilder und Texte sind entweder vom Autor selbst fotografiert oder verfasst oder sind gemeinfrei, es sei denn, es ist eine andere Quelle angegeben. Die gesammelten/vollständigen Literaturverzeichnisse der einzelnen Versuche sind jeweils in den entsprechenden Gesamtprotokollen zu finden.
Haftungsausschluss: Die Benutzung der hier vorliegenden Informationen geschieht auf vollkommen eigene Verantwortung. Haftung für Schäden oder Verluste, die beim Umgang mit den hier beschriebenen Stoffen oder bei der Durchführung von chemischen Versuchen entstehen, ist ausgeschlossen; ebenso wie Schadensersatzforderungen oder Gewährleistungsansprüche aufgrund falscher oder fehlender Angaben. Die Angaben zu den Stoffen und die Experimentieranleitungen wurden jedoch sorgfältig und nach bestem Gewissen erstellt und sind in jedem Falle zu beachten.
