| Thema: Ester und Ether | Tags: Williamson-Ether-Synthese, Ether, | Klassenstufen: 11-12 | Versuchsart: LV |
Materialien
Magnetrührer mit Heizfunktion, pneumatische Wanne, 3-Hals-Rundkolben, Rückflusskühler, Thermometer, Stopfen, Messzylinder, Feststofftrichter, Spatel, Büchnertrichter, Saugflasche
Chemikalien
Ethanol, Natriumhydroxid, Salzsäure, Monochloressigsäure, Dichloressigsäure, Stärke
Durchführung
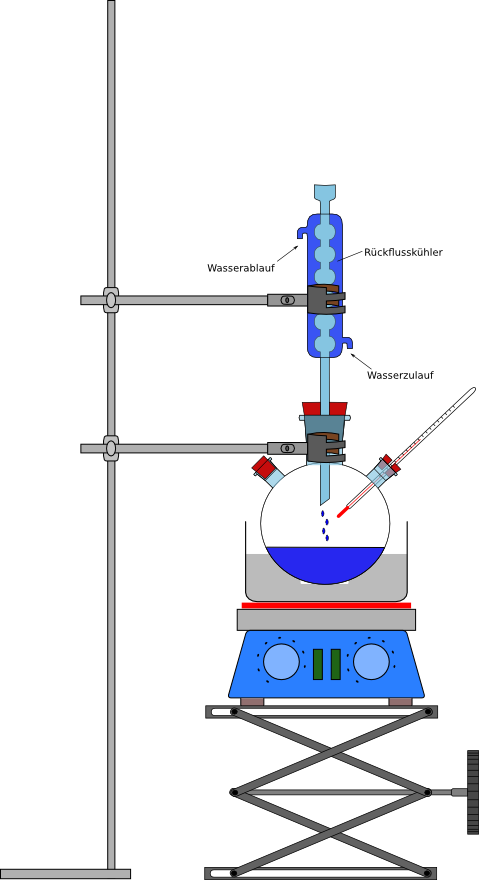
Zunächst wird die Apparatur gemäß Abb. 4 aufgebaut.
16,2 g Stärke, 100 mL Ethanol sowie 12 g Natriumhydroxid in 25 mL Wasser werden in den Rundkolben gegeben. Das Gemisch wird über 15 Minuten gerührt und anschließend eine Temperatur von 50 °C eingestellt. Das Gemisch wird weitere 20 Minuten gerührt.
9,4 g Monochloressigsäure werden hinzugeführt und 5 Minuten gerührt, bevor 2,6g Dichloressigsäure hinzugeführt werden und weitere 30 Minuten bei 50 °C gerührt wird.
Die abgekühlte Lösung wird abdekantiert und der Rückstand mit 50 mL Salzsäure versetzt. Der Rückstand wird zweimal mit Ethanol gewaschen und anschließend abfiltriert und eine Stunde bei 60°C getrocknet.
Das getrocknete Produkt wird fein zerrieben. In zwei Reagenzgläsern werden 2 g des Produktes bzw. 2 g Stärke mit jeweils 15 mL Wasser ver- setzt. Anschließend werden die Reagenzgläser geschüttelt.
Beobachtung
Durch die Zugabe von Mono- und Dichloressigsäure wird die Lösung viskoser. Durch Zusatz von Salzsäure fällt ein weißer Feststoff aus.
Beim Schütteln mit Wasser entsteht in dem Reagenzglas ein festes Gel. In dem Reagenzglas mit Stärke ist keine Löslichkeit und keine Gelbildung zu beobachten.
Deutung
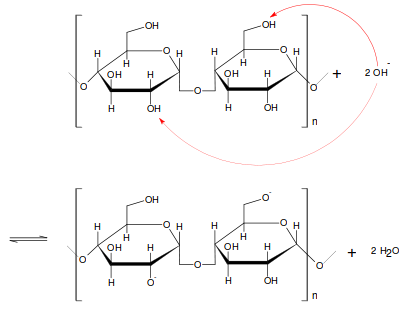
Stärke ist ein Polysaccharid, das aus Glucoseeinheiten aufgebaut ist. In Abbildung 1 werden Hydroxygruppen hervorgehoben, die durch Zugabe von Natriumhydroxid deprotoniert werden.
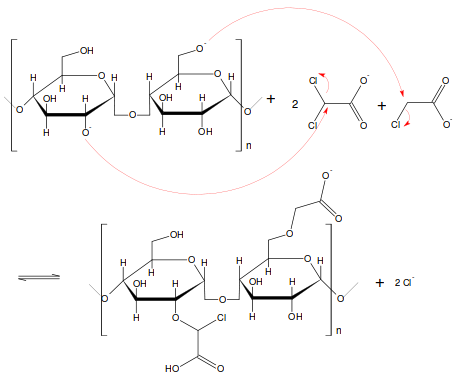
Über eine nucleophile Substitution (SN2) greift die Alkoholatgruppe die α- C-Atome der Mono- und Dichloressigsäuremoleküle an. Dabei entstehen Chloridionen und ein Ether (vgl. Abb. 2).
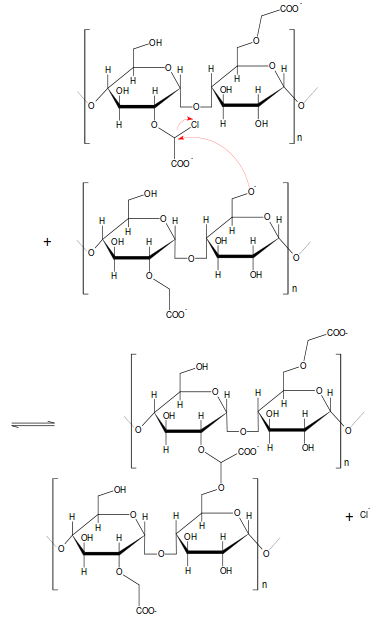
Die Dichloressigsäure kann ein weiteres Mal angegriffen werden. Dadurch entsteht ein dreidimensionales Netz.
Die absorbierende Wirkung des Produktes beruht auf den Carboxylgrup- pen. In Wasser werden diese deprotoniert und es entstehen Hydroxioniu- mionen. Innerhalb des Absorbers entsteht eine hohe negative Ladungs- dichte. Diese wird (analog zur Osmose) dadurch ausgeglichen, dass Was- sermoleküle in den Absorber diffundieren und dort durch Wasserstoffbrü- ckenbindungen gebunden werden.
Entsorgung
Stärke und das Produkt können im Haushaltsmüll entsorgt werden. Die bei der Reaktion entstehenden Flüssigkeiten werden über die organischen Abfälle entsorgt.
Der Versuch kann eingesetzt werden, um den Alltagsbezug organischer Reaktionsmechanismen zu verdeutlichen. Daher lässt sich auch die Williamson-Ether-Synthese mit diesem Versuch wiederholen.
Der Versuch eignet sich auch, um Kohlenhydrate und ihre möglichen Anwendungen zu diskutieren.
Der Versuch kann mit der entsprechenden Vorbereitung innerhalb einer Doppelstunde durchgeführt werden. Er zeigt damit auf, wie zeitintensiv organische Synthesen sein können. Eine Analyse der Eigenschaften des Reaktionsproduktes kann erst in der darauf folgenden Unterrichtsstunde vorgenommen werden, da das Produkt trocknen muss. In einem Kurs auf erweiterten Leistungsniveau erscheint dies möglich.
Literatur
[1] A. Gerner, http://www.chids.de/dachs/wiss_hausarbeiten/Kohlenhydrate_Gerner/Examensarbeit.pdf, S. 298-308, zuletzt abgerufen am 11.8.2013, 18.52 Uhr
Ähnliche Experimente
Ähnliche Experimente
Feedback
Haben Sie Anmerkungen, Feedback oder Kritik zu diesem Experiment? Kontaktieren Sie uns unter Bezugnahme auf diese Seite!
Copyright und Lizenzen: Alle Rechte an den Inhalten dieser eLearning-Materialien liegen beim Autor oder den jeweiligen Urheberrechtsinhabern. Sämtliche Bilder und Texte sind entweder vom Autor selbst fotografiert oder verfasst oder sind gemeinfrei, es sei denn, es ist eine andere Quelle angegeben. Die gesammelten/vollständigen Literaturverzeichnisse der einzelnen Versuche sind jeweils in den entsprechenden Gesamtprotokollen zu finden.
Haftungsausschluss: Die Benutzung der hier vorliegenden Informationen geschieht auf vollkommen eigene Verantwortung. Haftung für Schäden oder Verluste, die beim Umgang mit den hier beschriebenen Stoffen oder bei der Durchführung von chemischen Versuchen entstehen, ist ausgeschlossen; ebenso wie Schadensersatzforderungen oder Gewährleistungsansprüche aufgrund falscher oder fehlender Angaben. Die Angaben zu den Stoffen und die Experimentieranleitungen wurden jedoch sorgfältig und nach bestem Gewissen erstellt und sind in jedem Falle zu beachten.