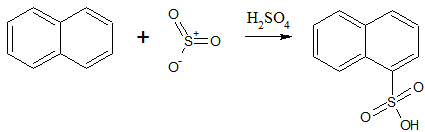| Thema: Aromaten | Tags: elektrophil, Substitution, Aromat, Sulfonierung | Klassenstufen: 11-12 | Versuchsart: SV |
Materialien
Mörser und Pistill, Reagenzglas, Bunsenbrenner, Becherglas
Chemikalien
Naphthalin, konz. Schwefelsäure, demineralisiertes Wasser
| Gefahrstoff | H-Sätze | P-Sätze | GHS |
|---|---|---|---|
| Naphthalin | H351-H302-H410 | -- |    |
| Schwefelsäure konz. | H314 | -- |  |
Durchführung
Etwa 1 g Naphthalin wird in einem Mörser zerrrieben und eine Spatelspitze davon in eine Reagenzglas gegeben. Dazu werden etwa 5 mL konzentrierte Schwefelsäure gegeben und erhitzt. Der Inhalt des Reagenzglases wird anschließend in ein Becherglas mit 50 mL demineralisertem Wasser gegeben.
Beobachtung
Die Lösung färbt sich beim Erhitzen rot-braun und löst sich gut im Wasser im Gegensatz zum Naphthalin.
Deutung
Das Naphthalin hat mit der Schwefelsäure reagiert. Dabei fand eine elektrophile Substitution mit einer Sulfit-Gruppe statt. Diesen Prozess nennt man Sulfonierung (vgl. Abb. 2). Das Sulfit entsteht aus der Autoprotolyse der Schwefelsäure.
Entsorgung
Die Lösung kann in den Abfallbehälter für organische Lösungsmittelabfälle gegeben werden.
Literatur
Jäckel, M. (u.a.) (Hrsg.), Chemie heute - Sekundarstufe II, Schroedel-Verlag, S.351
Ähnliche Experimente
Ähnliche Experimente
Feedback
Haben Sie Anmerkungen, Feedback oder Kritik zu diesem Experiment? Kontaktieren Sie uns unter Bezugnahme auf diese Seite!
Copyright und Lizenzen: Alle Rechte an den Inhalten dieser eLearning-Materialien liegen beim Autor oder den jeweiligen Urheberrechtsinhabern. Sämtliche Bilder und Texte sind entweder vom Autor selbst fotografiert oder verfasst oder sind gemeinfrei, es sei denn, es ist eine andere Quelle angegeben. Die gesammelten/vollständigen Literaturverzeichnisse der einzelnen Versuche sind jeweils in den entsprechenden Gesamtprotokollen zu finden.
Haftungsausschluss: Die Benutzung der hier vorliegenden Informationen geschieht auf vollkommen eigene Verantwortung. Haftung für Schäden oder Verluste, die beim Umgang mit den hier beschriebenen Stoffen oder bei der Durchführung von chemischen Versuchen entstehen, ist ausgeschlossen; ebenso wie Schadensersatzforderungen oder Gewährleistungsansprüche aufgrund falscher oder fehlender Angaben. Die Angaben zu den Stoffen und die Experimentieranleitungen wurden jedoch sorgfältig und nach bestem Gewissen erstellt und sind in jedem Falle zu beachten.