| Thema: Aktivierungsenergie und Katalysatoren IV | Tags: Aktivierungsenergie, exotherme Reaktion, Thermitreaktion | Klassenstufen: 7-8 | Versuchsart: LV |
Materialien
2 Blumentöpfe mit Loch, Papierhülse, Mörser mit Pistill, Filterpapier, Wunderkerze, Sand, Dreifuß
Chemikalien
Aluminiumpulver, Eisen(III)-oxid, Bariumperoxid, Magnesiumpulver
| Gefahrstoff | H-Sätze | P-Sätze | GHS |
|---|---|---|---|
| Eisen(III)-oxid rot | H315-H319-H335 | P261-P305+P351+P338 |  |
| Aluminium fein gepulvert | H261-H228 | -- |  |
| Eisen | Leider in der Datenbank nicht gefunden - bitte nachschlagen! | ||
| Bariumperoxid | H272-H332-H302 | -- |   |
| Magnesium | H228-H261-H252 | -- |  |
Durchführung
WICHTIG: Der Versuch darf nur draußen durchgeführt werden!
Das Thermitgemisch besteht aus 20 g Eisen(III)-oxid und 7 g Aluminiumpulver. Beides wird mit dem Mörser verrieben und in die Papierhülse überführt. Auf das Thermitgemisch wird die Zündmischung gegeben. Diese besteht aus 4 g Bariumperoxid und 6 g Magnesiumpulver.
WICHTIG! Die Zündmischung muss vorsichtig gemischt werden, auf keinen Fall im Mörser!
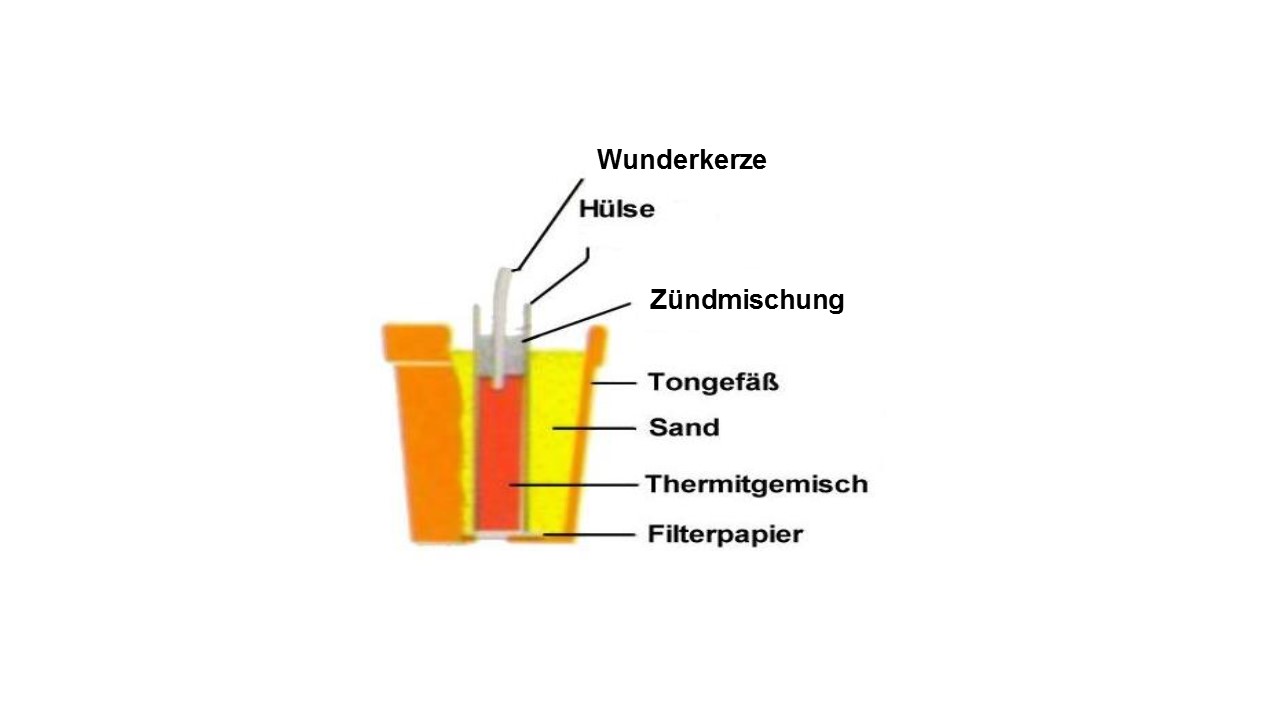
In die Papierhülse wird verkehrt herum eine Wunderkerze gesteckt. Die Blumentöpfe werden ineinander gestellt und auf das Loch im Blumentopf wird ein Filterpapier gebracht. Dieses wird mit ein wenig Sand bedeckt. Anschließend wird die Papierhülse mittig im Topf platziert und ebenfalls mit Sand umgossen. Die Töpfe werden nun in den Dreifuß gestellt. Die Wunderkerze kann nun gezündet werden und alle Versuchspersonen sollten sich in 3 m Entfernung zum Blumentopf befinden und ihre persönliche Schutzkleidung tragen.
Falls die Zündung versagt, muss mindestens 5 Minuten gewartet werden, bis der Versuch mit einer neuen Wunderkerze wiederholt werden kann.
Beobachtung
Nachdem die Wunderkerze gezündet wurde und zur Papierhülse runter brennt. Ist ein heller grüner Lichtblitz zu beobachten und Funken sprühen. Zusätzlich läuft eine Flüssigkeit aus dem Boden des Blumentopfs.
Deutung
Die Zündmischung liefert eine hohe Aktivierungsenergie, welches die Thermitreaktion auslöst. Es handelt sich in diesem Versuch um eine Redoxreaktion, in der Eisen(III)-oxid durch Aluminium zu Eisen reduziert wird. Zusätzlich handelt es sich um eine stark exotherme Reaktion, bei der sehr viel Energie freigesetzt wird. Dies wird durch die Beobachtung bestätigt. Da der erweiterte Redoxbegriff erst in den Höherenklassenstufen eingeführt wird, kann auf eine Symbolsprache verzichtet werden und nur die Wortgleichung aufgeschrieben werden.
Entsorgung
Die entstandenen Feststoffe werden im Feststoffabfall entsorgt.
Literatur
[1] R. Herbst-Irmer, Praktikumsskript zum Anorganischen Grundpraktikum für Lehramtskandidaten, 2014, S. 243.
Feedback
Haben Sie Anmerkungen, Feedback oder Kritik zu diesem Experiment? Kontaktieren Sie uns unter Bezugnahme auf diese Seite!
Copyright und Lizenzen: Alle Rechte an den Inhalten dieser eLearning-Materialien liegen beim Autor oder den jeweiligen Urheberrechtsinhabern. Sämtliche Bilder und Texte sind entweder vom Autor selbst fotografiert oder verfasst oder sind gemeinfrei, es sei denn, es ist eine andere Quelle angegeben. Die gesammelten/vollständigen Literaturverzeichnisse der einzelnen Versuche sind jeweils in den entsprechenden Gesamtprotokollen zu finden.
Haftungsausschluss: Die Benutzung der hier vorliegenden Informationen geschieht auf vollkommen eigene Verantwortung. Haftung für Schäden oder Verluste, die beim Umgang mit den hier beschriebenen Stoffen oder bei der Durchführung von chemischen Versuchen entstehen, ist ausgeschlossen; ebenso wie Schadensersatzforderungen oder Gewährleistungsansprüche aufgrund falscher oder fehlender Angaben. Die Angaben zu den Stoffen und die Experimentieranleitungen wurden jedoch sorgfältig und nach bestem Gewissen erstellt und sind in jedem Falle zu beachten.
